
河南省腫瘤醫院接受國食品藥品監督管理局核查(馮雷 攝)
【文匯網訊】(香港文匯網記者 馮雷)記者11月19日從河南省腫瘤醫院獲悉,日前,中國本土自主研發的百濟神州抗癌藥BRUKINSA™(澤布替尼)的上市申請獲美國食品藥品監督管理局批准。這是第一個在美國獲批上市的中國本土自主研發的抗癌藥,改寫了中國抗癌藥「只進不出」的歷史。
11月15日,美國食品藥品監督管理局批准百濟神州抗癌藥BRUKINSA™的上市申請。此次獲批主要基於一項在中國完成的、由北京大學腫瘤醫院牽頭、河南省腫瘤醫院等全國13家中心聯合進行的治療復發或難治性套細胞淋巴瘤(MCL)臨床試驗(簡稱206項目)。
河南省腫瘤醫院於2017年5月啟動該項目。套細胞淋巴瘤發病率低,試驗入組條件要求嚴格。以該院血液科主任醫師周可樹為主要研究者的研究團隊的努力下,該院在不到4個月的時間內,共篩選18例受試者,成功入組14例,以高速度、高質量協助全國提前完成入組,入組量排名全國第二,為該研究做出了突出貢獻。
百濟神州在美國申請該藥上市,鑒於該項目的重要性及河南省腫瘤醫院的入組數量較多。河南省腫瘤醫院血液科主任醫師、該項目主要研究者周可樹告訴記者,該院作為中國區兩家待查中心之一,率先接受美國食品藥品監督管理局核查。
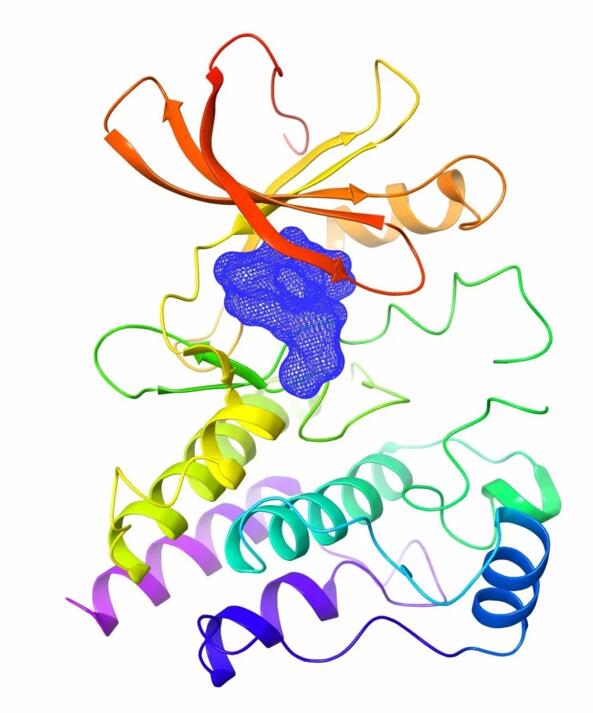
澤布替尼與BTK蛋白複合物晶體結構圖(截圖)
在為期三天半的核查過程中,美國食品藥品監督管理局核查員詳細核查試驗的整個流程、GCP藥房,對該項目的知情同意書和倫理批件逐一審閱,並對研究者文件夾、全部受試者文件夾展開核查。
他們抽查發藥還藥記錄、查看受試者的病歷,並著重對病歷中的AE記錄、體格檢查、試驗室報告、生命體征記錄、入排標準等內容進行核對;在核查期間,核查員對於河南省腫瘤醫院受試者的來源、受試者知情過程、該項目主要研究者如何參與受試者篩選/入組過程、血樣收集過程、以及影像評估判斷等方面提出問題。
本次核查順利通過,美國食品藥品監督管理局核查員對河南省腫瘤醫院的項目流程管理、文件記錄、藥房管理及該項目主要研究者及研究團隊的嚴謹工作作風表示讚賞。主核查員表示:「研究流程符合規範,數據客觀真實可靠,中心研究者認真負責,在患者篩選、用藥、療效評價、隨訪管理等諸多工作中表現優異,符合美國食品藥品監督管理局要求。」
作為河南省委、省政府確定的國家癌症區域醫療中心主體建設單位,河南省腫瘤醫院積極搭建科研平台,完善管理機制,培養科研學術帶頭人,打造高水平科研團隊,取得長足的進步。自2017年以來,該院先後8次迎接國家藥品監督局食品藥品審核查驗中心核查,得到核查員對該院臨床試驗質量的高度認可。
河南省腫瘤醫院黨委書記、院長張建功說,此次以零發現順利通過美國食品藥品監督管理局核查,是該院臨床試驗發展過程的一個重要里程碑,表明該院臨床試驗工作已達到較高水平,這將為他們轉型發展提供有力引領,助力臨床研究與臨床轉化,為更多的腫瘤患者帶來新希望。
責任編輯:滅白

